Discovery : intérêt et éthique des essais cliniques randomisés dans le contexte Covid-19
Publié en ligne le 5 décembre 2020 - Covid-19 -
Aucun traitement antiviral efficace contre le virus SARS-CoV-2 n’était disponible en janvier 2020, date de la prise en charge des premiers cas de Covid-19 en Europe. Aucun traitement antiviral n’était non plus validé contre les infections aux autres coronavirus émergents : syndrome respiratoire aigu sévère (lié au coronavirus SARS-CoV) ou syndrome respiratoire du Moyen-Orient (lié au coronavirus MERS-CoV). La communauté médicale se trouvait alors dans une situation qualifiée « d’équipoise clinique », c’est-à-dire dans une situation où « il existe une réelle incertitude au sein de la communauté médicale experte – pas nécessairement de la part de l’investigateur individuel – quant au traitement préféré » [1]. Les seules données disponibles, quelques semaines après la découverte du SARS-CoV-2, étaient des données d’efficacité antivirale in vitro pour certaines molécules candidates.
Essais cliniques ou études observationnelles ?

Dans cette situation d’équipoise, la communauté scientifique et médicale internationale recommande que des essais cliniques randomisés soient menés de façon rigoureuse afin de confirmer ou d’infirmer l’efficacité de ces traitements candidats et d’évaluer leur potentielle toxicité chez les patients. Pour apporter des réponses fiables, ces essais doivent comparer des stratégies thérapeutiques comportant les traitements candidats avec des stratégies thérapeutiques ne comportant pas les traitements candidats (essai « contrôlé ») en s’appuyant sur l’attribution aléatoire entre les groupes (essai « randomisé »). Il est possible, de façon exceptionnelle, de déroger à ce type d’évaluation en cas de traitement réputé a priori très efficace, notamment dans les maladies avec une morbidité et une mortalité très élevées comme cela a été le cas pour les patients multi résistants au virus du sida (VIH) au début des années 2000 avec un taux très élevé d’échec virologique [2] ou pour les patients atteints de fièvres hémorragiques comme la maladie à virus Ebola chez qui la mortalité est supérieure à 50 %. L’Organisation mondiale de la santé (OMS) qui commentait cette situation soulignait « le devoir moral » de la mise en œuvre d’essais cliniques rigoureux « afin de fournir les preuves de l’innocuité et de l’efficacité, ou, au contraire, les preuves devant conduire à arrêter le traitement » [3]. Cependant, il est important de noter que c’est finalement un essai clinique randomisé contrôlé qui a permis de modifier l’équipoise clinique (c’està-dire lever l’incertitude scientifique) pour la maladie à virus Ebola en identifiant un traitement efficace [4].
Pour la Covid-19, les premières données disponibles en provenance de Chine, et notamment celles présentées dans le premier article scientifique de grande ampleur rassemblant les données de 44 672 cas [5], ont montré que c’était une maladie virale aiguë – certes sévère – mais qui était associée à une symptomatologie modérée dans 81 % des cas. La mortalité globale était estimée à 2,3 % dans cette étude. Aujourd’hui, avec l’élargissement du dépistage qui conduit à l’identification des formes asymptomatiques ou peu symptomatiques, l’estimation du taux de mortalité est encore plus faible, évalué en France à 0,5 % [6]. Nous n’étions clairement pas dans les situations évoquées plus haut et il était donc incontournable de procéder à des essais cliniques rigoureux, en ciblant tout d’abord la population qui pouvait en tirer le plus grand bénéfice, c’est-à-dire les patients hospitalisés.
Les essais cliniques randomisés constituent le plus haut niveau de preuve dans la littérature médicale et scientifique pour le choix des prises en charge thérapeutiques [7], qu’elles soient médicamenteuses ou non médicamenteuses. Ils ne s’opposent pas aux autres modalités d’évaluation thérapeutique qui peuvent être conduites en parallèle et apporter des réponses préliminaires si leur méthodologie est de qualité. C’est notamment le cas des études observationnelles comportant un groupe contrôle comparable au groupe traité 1. Cependant, les résultats provenant d’études non randomisées doivent toujours être confirmés ou infirmés par des études de niveau supérieur en termes de niveau de preuve avant de prescrire largement des traitements. Comme le soulignent l’Académie nationale de médecine, l’Académie nationale de pharmacie et l’Académie des sciences, « en période de pandémie aussi bien qu’en situation ordinaire, les règles de l’évaluation critique des méthodes et des résultats doivent s’appliquer. Il en est de même de la déontologie scientifique et médicale, du respect de l’intégrité scientifique et de l’éthique de la communication des résultats » [8].
C’est pourquoi l’OMS recommande [9] depuis plusieurs années de mettre en place de grands essais cliniques randomisés collaboratifs et internationaux pour faire face aux maladies émergentes et évaluer au mieux les stratégies préventives et thérapeutiques les plus prometteuses. Cette analyse de la situation a conduit à la mise en place d’essais cliniques randomisés de grande ampleur chez les patients atteints de Covid-19 et hospitalisés. Notons en particulier la Chine, le Royaume-Uni, les États-Unis, les pays européens participants à Discovery ou les 21 pays participant effectivement à l’essai clinique Solidarity mis en œuvre par l’OMS [10].
La création de Discovery
Dès fin janvier 2020, alors que les premiers cas de patients atteints de Covid-19 étaient identifiés en France et en Europe, le consortium
REACTing de l’Inserm est entrée en contact avec l’OMS avec une proposition de mettre en place un essai clinique randomisé contrôlé afin d’évaluer les options thérapeutiques contre la Covid-19 pour les patients hospitalisés. Les réflexions menées au sein de REACTing, avec des partenaires européens et avec l’OMS, ont donné naissance à l’essai thérapeutique Discovery [11] dont l’objectif était d’évaluer l’efficacité et la sécurité de molécules antivirales repositionnées (c’est-à-dire de traitements enregistrés ou évalués initialement pour d’autres maladies) pour le traitement de la Covid-19. Discovery a débuté en France en mars 2020 pour ensuite s’étendre à l’Europe et est intimement lié à Solidarity. Discovery est un essai clinique dit « fille » de Solidarity, c’est-à-dire qu’il évalue les mêmes stratégies thérapeutiques et que certains de ses critères de jugement, comme le taux de mortalité, sont alignés sur ceux de Solidarity.
Les molécules candidates ont été sélectionnées au cours d’une série de consultations conduites pendant la période janvier-février 2020 par un groupe pluridisciplinaire de l’OMS sur la base de différents arguments :
- le fait que ces molécules soient déjà en cours d’évaluation dans des maladies virales proches, comme c’est le cas pour l’interféron pour le syndrome respiratoire du Moyen-Orient ;
- de données in vitro suggérant une potentielle activité antivirale sur les coronavirus et sur SARS-CoV-2 [12] ;
- de données préliminaires obtenues dans des modèles animaux infectés par le SARS-CoV-2 ;
- de premières données cliniques issues d’études non contrôlées (en provenance notamment de Chine).
Dès février 2020, trois candidats thérapeutiques ont émergé : le remdésivir, l’association lopinavir/ritonavir et l’interféron ß-1. Par la suite, début mars 2020, l’hydroxychloroquine a été ajoutée à ces traitements candidats sur la base de nouvelles données préliminaires. Discovery est un essai clinique adaptatif, c’est-à-dire que les molécules candidates peuvent être changées sur recommandation du comité indépendant de surveillance et de suivi des résultats. Ainsi, une molécule peut devenir le standard de soins si son efficacité est prouvée supérieure aux autres traitements, l’évaluation d’une molécule peut être interrompue si son efficacité s’avère inférieure aux autres ou en cas de toxicité, des bras de traitement peuvent être ajoutés en cas de nouvelles stratégies thérapeutiques identifiées. Le protocole complet de Discovery a été soumis et publié dans une revue scientifique en open access (libre accès) [11].
Une mise en place rapide dans un contexte pandémique
Le recours à des essais cliniques rigoureux a parfois été contesté au nom des supposées lenteurs et lourdeurs qu’ils impliqueraient. La mise en place du protocole de Discovery a été initiée fin février 2020. Moins d’un mois a été nécessaire pour adapter le « master protocol » (protocole initial) de l’OMS, obtenir les autorisations réglementaires du Comité de protection des personnes (CPP) et de l’Agence nationale de sécurité du médicament (ANSM), autorisation initiale le 6 mars 2020, obtenir un fonds d’amorçage via le module Inserm REACTing après passage devant un comité scientifique indépendant créé dès le mois de janvier 2020. Le premier patient a été inclus dans Discovery le 22 mars 2020. Le financement par le Programme hospitalier de recherche clinique (PHRC) du ministère des Solidarités et de la Santé de cette étude a été obtenu le 25 mars 2020.
Les ouvertures de 32 centres se sont succédé de façon très rapide dans des conditions inhabituelles à tout point de vue : praticiens investigateurs, praticiennes investigatrices et leurs équipes, surchargés par les activités de soins, complexité d’un essai randomisé à cinq bras. Néanmoins, et avec un calendrier d’ouverture des centres calqué sur la dynamique géographique de l’épidémie, l’inclusion des malades a été particulièrement rapide (268 malades inclus à la fin de la première semaine, 533 à 15 jours et 700 à un mois). Ensuite, l’inclusion des patients s’est ralentie compte tenu de l’initiation d’autres essais cliniques (et l’impossibilité d’inclure simultanément les patients dans deux essais cliniques distincts) mais aussi suite à la diminution du nombre d’hospitalisations pour Covid-19. Le mardi 1er septembre 2020, 875 patients étaient inclus dans l’essai Discovery.
Un essai clinique national puis européen
Dès les premières étapes de Discovery, la volonté a été d’inviter d’autres pays européens qui n’avaient pas mis en place d’essai clinique randomisé de grande ampleur à participer à Discovery (soit la grande majorité des pays européens en dehors du Royaume-Uni avec son essai Recovery [13]). Ceci a permis de prévoir l’inclusion de 800 patients en France et de 2 300 patients dans le reste de l’Union européenne. Cependant, le déploiement d’un tel essai au niveau européen s’est avéré plus complexe que prévu malgré l’identification rapide des investigateurs intéressés dans chaque pays. En effet, il est nécessaire de tenir compte des différences réglementaires d’un pays à l’autre, de trouver les financements et de prendre en compte les spécificités et les choix de chaque pays (les médicaments à évaluer et les modes de recueil de données en particulier). Alors que les autorisations réglementaires ont été obtenues très rapidement en France, grâce à une réactivité exemplaire des agences sanitaires, ceci n’a pas été le cas dans d’autres pays européens. Les trois académies françaises (médecine, pharmacie, sciences) se sont d’ailleurs prononcées en demandant « qu’une coordination des essais et une standardisation des procédures (conditions, conduite, évaluation, enregistrement, communication) soient instaurées au niveau européen » [8].
L’intégration dans l’essai Solidarity organisé par l’OMS
Dès le 29 mars 2020, Discovery a accepté de devenir un essai « fille » de l’essai clinique mondial Solidarity mené par l’OMS et qui évalue les mêmes stratégies thérapeutiques chez les patients hospitalisés pour Covid-19. Les données cliniques de chaque patient inclus dans Discovery sont transmises à Solidarity pour analyse consolidée avec les données fournies par les autres pays.
À ce jour, 21 pays dans le monde contribuent à l’essai Solidarity et la France, grâce à Discovery, est le deuxième pays contributeur en nombre de patients (sur les presque 6 000 patients de Solidarity au 8 juillet 2020, 776 étaient des patients français de Discovery). Cette collaboration permet d’assurer que les données de tous les patients inclus dans Discovery contribueront à une initiative plus grande bénéficiant du nombre de sujets nécessaires pour apporter des preuves définitives d’efficacité ou d’inefficacité sur des critères de jugement comme la mortalité. Par ailleurs, l’essai Discovery a une importance particulière pour Solidarity puisqu’il recueille des données plus fines et plus précises, notamment concernant la virologie, la pharmacologie (concentration des médicaments) ou les effets indésirables des traitements. Discovery est ainsi le seul essai clinique du consortium Solidarity de l’OMS à évaluer de façon extrêmement rigoureuse tous les effets indésirables, dont les effets indésirables sévères, permettant de recueillir des données de pharmacovigilance précieuses afin de savoir si les stratégies thérapeutiques ne sont pas plus délétères qu’elles ne sont bénéfiques.
Les difficultés rencontrées
Parmi les difficultés rencontrées, signalons : un déploiement logistique complexe pendant le confinement, un nombre important de sites hospitaliers à ouvrir en urgence dans un temps très restreint, l’activation synchronisée d’une filière médicale et d’une filière de réanimation par centre afin d’inclure des patients avec des niveaux de sévérité différents, la tension autour des stocks de médicaments avec quatre molécules différentes testées – dont le remdésivir qu’il a fallu faire venir des États-Unis –, l’initiation et la concurrence d’autres essais cliniques [14], l’inclusion de partenaires européens ralentie par des contraintes notamment réglementaires différentes entre les pays et par l’absence d’une stratégie anticipée et partagée sur le plan scientifique, enfin une pression médiatique forte liée à l’attente pressante de résultats.

De plus, comme cela a été signalé à de nombreuses reprises, les inclusions de patients dans Discovery ont été freinées par une communication généralisée dans les médias qui évoquait une efficacité spectaculaire de l’hydroxychloroquine, à une période où l’ensemble de la communauté médicale et scientifique internationale reconnaissait qu’il n’y avait pas suffisamment d’éléments pour se prononcer définitivement sur les bienfaits de ce traitement. Dans ce contexte, et sous couvert d’un décret ministériel transitoire permettant la prescription d’hydroxychloroquine, de nombreux patients ont été traités par cette dernière avant leur arrivée à l’hôpital et ne pouvaient donc pas être inclus dans un essai visant à évaluer l’efficacité de traitements antiviraux (il était en effet impossible dans ce cas de figure de faire la différence entre l’effet potentiel de l’hydroxychloroquine donnée avant inclusion et l’effet du traitement administré dans le cadre de l’essai). Enfin, d’autres patients ont refusé l’inclusion dans Discovery parce qu’ils désiraient bénéficier uniquement d’un traitement par hydroxychloroquine.
Conclusion
Les essais randomisés contrôlés sont indispensables dans un contexte pandémique afin d’obtenir des réponses fiables sur les candidats thérapeutiques. Les études observationnelles peuvent faire émerger des hypothèses thérapeutiques, mais celles-ci doivent ensuite être confirmées par des essais randomisés. La rigueur scientifique a un coût, mais c’est la seule voie permettant de tirer des conclusions applicables sur le plan thérapeutique à même de convaincre des médecins partout dans le monde [15].
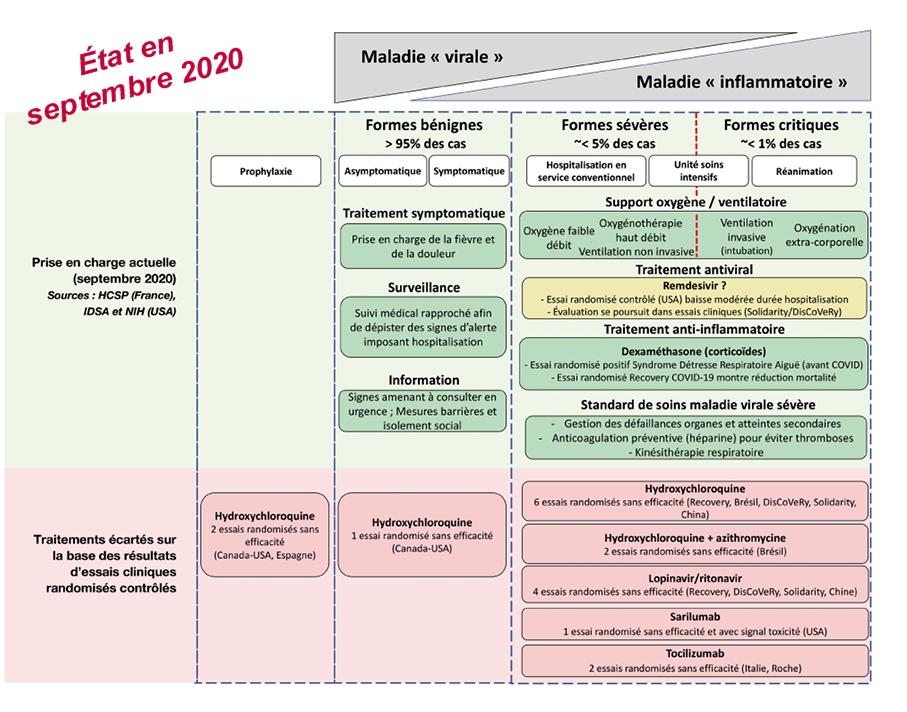
À ce jour, bien qu’encore très incomplète, la connaissance scientifique s’est consolidée grâce aux différents essais cliniques menés à l’échelle internationale (voir figure).
1 | Freedman B, “Equipoise and the Ethics of Clinical Research”, N Engl J Med, 1987, 317 :141-5.
2 | Yazdanpanah Y et al., “High rate of virologic suppression with raltegravir plus etravirine and darunavir/ritonavir among treatment-experienced patients infected with multidrug-resistant HIV : results of the ANRS 139 TRIO trial”, Clin Infect Dis, 2009, 49 :1441-9.
3 | Organisation mondiale de la santé,“Ethical considerations for use of unregistered interventions for Ebola virus disease”, Report of an advisory panel to WHO, 2014. Sur who.int
4 | Mulangu S et al., “A Randomized, Controlled Trial of Ebola Virus Disease Therapeutics”, N Engl J Med, 2019, 381 :2293-303.
5 |Wu Z et al.,“Characteristics of and Important Lessons From the Coronavirus Disease 2019 (COVID-19) Outbreak in China”, JAMA, 2020, 323 :1239-42.
6 |Salje H et al., “Estimating the burden of SARS-CoV-2 in France”, Science, 2020, 369 :208-11.
7 |Djulbegovic B, Guyatt GH,“Progress in evidence-based medicine : a quarter century on”, The Lancet, 2017, 390 :415-23.
8 | « Essais cliniques au cours de la pandémie Covid-19 : Cibles thérapeutiques, exigences méthodologiques, impératifs éthiques », avis tri-académique (Académies nationales de médecine, de pharmacie et des sciences), 29 mai 2020.
9 |OMS, “Guidance for Managing Ethical Issues in Infectious Disease Outbreaks”, 2016. Sur who.int
10 |OMS, « Essai clinique “Solidarity” de traitements contre la COVID-19 », 2020. Sur who.int
11 | Ader F, on behalf of The DisCoVeRy French Trial Management Team,“Protocol for the DisCoVeRy trial : multi-centre, adaptive, randomized trial of the safety and efficacy of treatments for COVID-19 in hospitalized adults”, BMJ Open, 2020, 10 :e041437.
12 | Fragkou PC et al.,“Review of trials currently testing treatment and prevention of COVID" Clin Microbiol Infect, 2020, 26 :988-98.
13 | Site de l’essai clinique Recovery (Royaume-Uni) : recoverytrial.net
14 | Peiffer-Smadja N et al.,“Anticovid, a comprehensive open-access real-time platform of registered clinical studies for COVID-19”, J Antimicrob Chemother, 2020, 75 :2708-10.
15 | [ Ferry-Danini J, « Petite introduction à l’éthique des essais cliniques. Coronavirus – Réponse au Professeur Raoult », Medium, 1er avril 2020. Sur medium.com
1 Une étude observationnelle est une étude qui se base sur les données présentes dans le dossier médical des personnes étudiées ou les données collectées lors du traitement, en excluant toute intervention de l’investigateur. Elle peut comporter un groupe de comparaison (groupe contrôle). Le traitement dans chaque groupe est celui choisi par l’investigateur dans la prise en charge et les groupes peuvent donc être différents (il est fréquent que les patients pour lesquels les médecins choisissent d’introduire un traitement soient différents de ceux chez qui les médecins choisissent de ne pas en mettre).
Publié dans le n° 334 de la revue
Partager cet article
Les auteurs

Yazdan Yazdanpanah
Chef du service de maladies infectieuses et tropicales de l’hôpital Bichat – Claude Bernard et coordinateur de (…)
Plus d'informations
Nathan Peiffer-Smadja
Nathan Peiffer-Smadja est Docteur en médecine, spécialisé en maladies infectieuses et tropicales, étudiant en thèse (…)
Plus d'informationsCovid-19

Science, expertise et décision à l’épreuve de la pandémie de Covid-19
Le 15 juillet 2020
Covid-19, hydroxychloroquine et traitement médiatique
Le 9 janvier 2023
Mauvaises conduites et Covid-19
Le 11 octobre 2022
Restaurer l’intégrité scientifique après la crise Covid-19
Le 4 octobre 2022Communiqués de l'AFIS















![[16 juin 2022 - Paris] Covid-19 : Deux ans d'épidémie, qu'avons-nous appris ?](local/cache-gd2/0f/33c69087dceb597afeb0e562895a7f.jpg?1675291840)