Le glyphosate est-il cancérogène ?
Publié en ligne le 16 février 2018 - Pesticides -
Le glyphosate est une substance active d’herbicide couramment employée en agriculture et qui est au centre d’une âpre controverse quant à sa dangerosité. Depuis sa mise sur le marché en 1974, il a fait l’objet d’un très grand nombre d’études scientifiques à travers le monde concernant son mode d’action, son efficacité, sa toxicité, son écotoxicité, son caractère mutagène, cancérogène, reprotoxique (toxique pour la reproduction) ou perturbateur endocrinien.

Le moteur de recherche d’articles scientifiques Google Scholar renvoie plus de 200 000 résultats sur la requête « glyphosate », ce qui indique que la recherche scientifique mondiale a été très active autour de cette substance.
Pourtant, le Centre international de recherche sur le cancer (CIRC, une des agences dépendant de l’OMS) a jeté un pavé dans la mare en déclarant le glyphosate « cancérogène probable » pour l’Homme (groupe 2A) dans un avis publié le 20 mars 2015. Cette annonce interpelle. Comment se fait-il qu’aucune agence de sécurité sanitaire au monde n’ait reconnu le moindre caractère cancérogène au glyphosate durant plus de quarante ans ? De nouvelles données, analysées par le CIRC, auraient-elles permis de révéler une vérité ignorée depuis des décennies ?
Dès l’annonce du CIRC, plusieurs gouvernements à travers le monde ont demandé à leurs agences sanitaires réglementaires de mener en urgence une réévaluation du potentiel cancérogène du glyphosate. Dans le même temps, de nombreux articles de presse ont sonné le tocsin, affirmant ici que l’OMS aurait déclaré le glyphosate cancérogène, prévoyant là un nouveau scandale sanitaire à venir, évoquant ailleurs les scandales de l’amiante ou du médiator. Pendant ce temps, les réseaux sociaux s’agitaient sur le thème « on ne nous dit pas tout », regrettant que la santé des citoyens soit mise en péril par le laxisme des gouvernements et des agences sanitaires ayant autorisé la molécule maudite au profit de quelques multinationales influentes. Dans la foulée, des personnalités publiques, des organisations non gouvernementales, des partis politiques, ont exigé l’interdiction rapide de l’emploi des herbicides à base de glyphosate.
Cette affaire devait être éclaircie. C’est la tâche que nous nous sommes fixée dans le présent article. Néanmoins, nous ne nous prononcerons pas sur les questions relevant de décisions politiques, comme « faut-il interdire le glyphosate ? », « faut-il en sortir progressivement ? » ou, au contraire, « faut-il prolonger l’autorisation des herbicides contenant cette molécule ? ». Ces questions ne peuvent se réduire aux seules considérations scientifiques. Soucieux d’éclairer nos lecteurs, nous rassemblons ici les éléments relatifs à l’expertise existante sur la cancérogénicité du glyphosate. L’analyse est exigeante mais nécessaire à qui veut se faire une opinion fondée sur les faits 1.
L’évaluation de la sécurité sanitaire du glyphosate
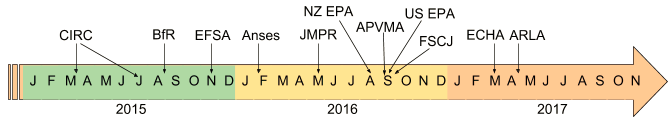
Suite à l’avis du CIRC, en deux ans et demi, une dizaine d’agences de sécurité sanitaire ont réétudié le potentiel cancérogène du glyphosate. Pour le présent article, nous avons analysé, au 20 octobre 2017, les derniers avis publiés par onze instances publiques (Allemagne, Australie, Canada, États-Unis, Europe, France, Nouvelle-Zélande, Japon). Cela représente une vingtaine de rapports d’expertise, pour un total d’environ 1 500 pages.
– CIRC, Centre international de recherche sur le cancer, 20 mars 2015
– BfR, Agence allemande de sécurité sanitaire, 31 août 2015
– EFSA, Autorité européenne de sécurité alimentaire, 12 novembre 2015
– Anses, Agence française de sécurité sanitaire, 9 février 2016
– JMPR, Réunion mixte de la FAO et de l’OMS sur les résidus de pesticides, 16 mai 2016
– NZ EPA, Autorité de protection de l’environnement de Nouvelle Zélande, août 2016
– APVMA, Autorité australienne des pesticides et médicaments vétérinaires, septembre 2016
– US EPA, Agence américaine de protection de l’environnement, 12 septembre 2016
– FSCJ, Commission japonaise de sécurité des aliments, 30 septembre 2016
– ECHA, Agence européenne des produits chimiques, 15 mars 2017
– ARLA, Agence canadienne de réglementation de la lutte antiparasitaire, 28 avril 2017
Établir le danger et évaluer le risque
Tous les pays industrialisés ont mis en place un réseau d’agences de sécurité sanitaire, financées sur fonds publics, ayant pour mission d’évaluer scientifiquement la sécurité sanitaire des produits chimiques, dont les pesticides. Elles mènent des expertises collectives fondées sur l’ensemble de la littérature scientifique.
Toutes les agences n’ont pas la même mission, ni le même rôle institutionnel. En particulier, l’établissement d’un danger et l’évaluation du risque associé sont séparés, et complémentaires. Une substance peut être dangereuse sans poser de risque sanitaire compte tenu de son utilisation ou de la faiblesse de l’exposition. L’évaluation du risque prendra également en compte des profils particuliers : utilisateurs résidentiels, agriculteurs, riverains, consommateurs, enfants, femmes enceintes, etc.
Ainsi, par exemple, le CIRC qui dépend de l’OMS effectue une classification des agents en fonction des connaissances scientifiques sur leur cancérogénicité. Les agents sont classés en cinq catégories : groupe 1 « cancérogène », groupe 2A « cancérogène probable », groupe 2B « cancérogène possible », groupe 3 « non classable », groupe 4 « non cancérogène ». Cependant le CIRC précise bien qu’il n’évalue pas l’impact sanitaire des agents qu’il classe, mais seulement un degré de connaissance : « La classification du CIRC indique la force des indications scientifiques disponibles quant à la cancérogénicité d’une substance. Il ne donne aucune indication sur le niveau de risque associé à l’exposition en question. Ainsi, si deux “agents” sont classés dans le même groupe, cela signifie que nous pouvons dire avec le même degré de certitude que [ces deux agents] peuvent provoquer le cancer, mais l’on ne peut pas dire à quel point chaque agent est dangereux ou à quelle dose il faudrait y être exposé pour que ces “agents” provoquent un cancer »[0]. C’est la distinction fondamentale entre « identification des dangers » et « évaluation des risques » en sécurité sanitaire.
Le JMPR (Réunion mixte de la FAO et de l’OMS sur les résidus de pesticides) complète en indiquant que « le travail du CIRC et du JMPR sont différents, bien que complémentaires, et leurs fonctions respectives peuvent être vues comme un continuum dans lequel les dangers potentiels pour la santé publique sont identifiés [par le CIRC] et le niveau de risque associé à ces dangers est ensuite évalué [par le JMPR] ». Autrement dit, au sein de l’OMS, le CIRC ne fait que mettre en lumière un danger potentiel, sans évaluer le niveau de risque associé. Pour les pesticides, le JMPR évalue ensuite le niveau de risque correspondant.
Une distinction entre identification de dangers et évaluation de risques existe aussi au sein des instances réglementaires européennes. L’ECHA, Agence européenne des produits chimiques, est chargée de la classification des substances dangereuses en Europe (règlement relatif à la classification, à l’étiquetage et à l’emballage – CLP), ses avis ayant une valeur réglementaire (contrairement à ceux du CIRC). La classification ne tient pas compte du niveau de l’exposition des populations à la substance. L’évaluation des risques des pesticides, en tenant compte du niveau d’exposition des utilisateurs, des résidents et des autres populations, est ensuite du ressort de l’Autorité européenne de sécurité des aliments (EFSA).
Un produit pesticide – désigné aussi comme « une formulation » – est composé d’une ou plusieurs substances actives et de coformulants. Par exemple, le Roundup de Monsanto a été le premier produit pesticide mis sur le marché contenant la substance active glyphosate. Au sein de l’Union européenne, ce sont les agences sanitaires de chaque État membre – l’Anses pour la France – qui ont la responsabilité d’évaluer un produit pesticide en vue de son autorisation sur leur territoire. De leur côté, en Europe, les agences communautaires (ECHA et EFSA) sont chargées d’évaluer les substances actives prises isolément. Si une substance active est interdite au niveau communautaire, toutes les formulations de produits pesticides la contenant seront interdites dans tous les États membres. Le contraire n’est pas vrai : un État membre peut choisir de ne pas autoriser une formulation de produit pesticide sur son territoire, même si les substances actives sont autorisées individuellement au niveau communautaire. Ainsi, il existe environ 2 000 produits herbicides utilisés dans l’Union européenne contenant la substance active « glyphosate », quelques centaines étant actuellement autorisés en France par l’Anses.
L’évaluation de la cancérogénicité
L’évaluation de la cancérogénicité d’un produit se base sur l’analyse de trois types d’éléments de preuve :
- génotoxicité (ou mutagénicité) ;
- cancérogénicité pour l’animal ;
- cancérogénicité pour l’Homme.
Génotoxicité
Une substance génotoxique (dite aussi mutagène) est susceptible d’abîmer l’ADN contenu dans les cellules. Cela n’aboutit pas toujours à un cancer, loin de là. Pour cela, encore faut-il que les mécanismes de réparation de l’ADN présents dans chaque cellule soient dépassés et que le système immunitaire ne parvienne pas non plus à éliminer les cellules anormales. C’est pourquoi la démonstration de la génotoxicité (dite aussi mutagénicité) d’une substance permet d’envisager des mécanismes de cancérogénèse possibles, mais est insuffisante pour soutenir son caractère cancérogène chez l’animal ou chez l’Homme.
Plusieurs centaines d’études scientifiques ont été menées pour évaluer le potentiel génotoxique du glyphosate. Beaucoup sont réalisées in vitro, sur divers types de cultures cellulaires dont des cellules humaines. D’autres sont réalisées in vivo, notamment sur des mammifères, modèle le plus pertinent pour extrapoler à l’Homme. L’évaluation du caractère génotoxique s’effectue en observant les éventuelles altérations des chromosomes et de l’ADN suite à une exposition ponctuelle au produit testé.
Cancérogénicité pour l’animal

La cancérogénicité pour l’animal est évaluée dans des études dites de « long terme » dans lesquelles un groupe d’animaux de laboratoire est exposé à la substance pendant une durée proche de leur durée de vie, environ deux ans pour les rats et souris. Un autre groupe, dit « témoin », ne reçoit pas ce traitement, tout en bénéficiant des mêmes conditions de vies. Ces études sont beaucoup moins nombreuses que les études de génotoxicité, car bien plus longues et coûteuses. L’évaluation du caractère cancérogène s’effectue en répertoriant les tumeurs sur l’ensemble des organes. Dans ces études, l’analyse statistique est primordiale pour comparer les résultats des comptages de tumeurs entre les groupes traités et témoins. En effet, tous les animaux, traités ou témoins, sont susceptibles de développer des tumeurs en fin de vie, ce qui rend délicate une attribution causale.
Cancérogénicité pour l’Homme
La cancérogénicité pour l’Homme est évaluée à l’aide d’études épidémiologiques. Ces études sont principalement de deux types : cas-témoins ou cohorte (voir encadré).
Les études épidémiologiques chez l’Homme
Étude cas-témoins. Une étude cas-témoins, dite aussi « rétrospective », consiste à considérer deux groupes de personnes : les « cas » et les « témoins ». Les cas sont des personnes atteintes d’une maladie donnée, un type de cancer par exemple. Le groupe « témoins » doit être similaire aux cas pour un ensemble de caractéristiques choisies (âge, sexe, mode de vie, etc.), mais sans être atteint de la maladie. Ensuite, les chercheurs essaient d’évaluer rétrospectivement l’exposition des membres des deux groupes aux produits à évaluer. L’analyse statistique permet de vérifier si les cas ont été davantage exposés au produit que les témoins.
Les études cas-témoins travaillent souvent sur un nombre réduit de personnes et sont sujettes aux « biais de rappel », car l’évaluation de l’exposition nécessite que les personnes se souviennent après coup de leur utilisation passée des produits, parfois sur des décennies. Il a aussi été démontré que les personnes atteintes de maladie ont tendance à surestimer leur exposition passée à un facteur qui leur est présenté comme potentiellement déterminant pour celle-ci, ce qui peut affaiblir les résultats des études cas-témoins.
Étude de cohorte. Une étude de cohorte, dite aussi « prospective », consiste à suivre un groupe de personnes sur une longue durée. Au fil des années, les chercheurs recensent le niveau d’exposition des participants aux produits à évaluer et répertorient leurs événements de santé. L’analyse statistique permet ensuite de contrôler si les personnes les plus exposées à un produit donné sont davantage atteintes de certaines maladies que les personnes moins exposées.
Les études de cohorte peuvent concerner un grand nombre de personnes (plusieurs dizaines de milliers), mais souvent, pour une maladie donnée, par exemple un type de cancer particulier, le nombre de cas reste petit dans la cohorte.
Par rapport aux études sur animaux, les études épidémiologiques ont l’inconvénient de ne pas permettre de discriminer facilement un facteur. Par exemple, les agriculteurs exposés aux herbicides à base de glyphosate sont souvent exposés à d’autres herbicides ou d’autres pesticides, aux rayons ultraviolets du soleil, aux gaz d’échappement des machines agricoles, rendant délicate la séparation de la responsabilité de chaque facteur. Les études épidémiologiques ne permettent pas non plus de séparer l’effet du glyphosate lui-même de celui des coformulants. En revanche, dans les études animales, la conception de l’étude permet de comparer deux groupes dont les conditions de vie ne diffèrent que par un seul facteur choisi, par exemple l’exposition au glyphosate, ce qui élimine les facteurs de confusion.
Finalement, c’est en considérant les niveaux de preuves pour les trois types d’études (génotoxicité, cancérogénicité animale et cancérogénicité humaine) que le potentiel cancérogène d’une substance est évalué.
Analyse des avis des agences sanitaires
Ce qui frappe à la lecture des avis des agences (voir encadré ci-dessous), c’est à quel point l’avis du CIRC tranche par rapport à tous les autres. Pour comprendre, on ne peut pas faire l’économie d’entrer dans le détail des analyses.
| Centre international de recherche sur le cancer (CIRC – OMS, 29 juillet 2015) [1] :
– « Il existe des preuves solides que le glyphosate cause une génotoxicité » (p. 77) – « Il existe des preuves suffisantes de cancérogénicité du glyphosate sur les animaux de laboratoire » (p. 78) – « Il existe des preuves limitées chez l’Homme de la cancérogénicité du glyphosate. Une association positive a été trouvée pour le lymphome non-hodgkinien » (p. 78) – « Le glyphosate est probablement cancérogène pour l’Homme (groupe 2A) » (p. 78). |
| Agence allemande de sécurité sanitaire (BfR, 31 août 2015) [6] :
– « Le glyphosate n’induit pas de mutations in vivo et aucune classification de risque de mutagénicité n’est justifiée selon les critères CLP » (Préface iii, Abstract) – « Le poids des preuves suggère qu’il n’y a pas de risque cancérogène lié aux usages prévus de l’herbicide et, en outre, qu’aucune classification de danger pour la cancérogénicité n’est justifiée pour le glyphosate selon les critères CLP » (Préface iii, Abstract). |
| Autorité européenne de sécurité alimentaire (EFSA, 12 novembre 2015) [3,4] :
– « En tenant compte de la qualité et de la fiabilité de toutes les données disponibles, l’évaluation par les pairs de l’EFSA a conclu qu’il est improbable que le glyphosate soit génotoxique in vivo et n’exige pas de classification de danger concernant la mutagénicité selon le règlement CLP [règlement relatif à la classification, à l’étiquetage et à l’emballage] » ([3] p. 3) – « Le glyphosate n’a pas présenté de potentiel génotoxique et aucune preuve de cancérogénicité n’a été observée chez le rat ou la souris » ([4] p. 10) – « L’EFSA a conclu qu’il est improbable que le glyphosate présente un danger cancérogène pour l’Homme et les éléments de preuves ne justifient pas de classification en ce qui concerne son potentiel carcinogène selon le règlement (EC) No 1272/2008 » ([4] p. 1) |
| Agence française de sécurité sanitaire (Anses, 9 février 2016) [7] :
– « Le niveau de preuve pour associer le glyphosate à un risque augmenté de lymphome non-Hodgkinien est limité chez l’Homme » (p. 4) – « Au vu de l’ensemble des résultats, le niveau de preuve de la génotoxicité du glyphosate chez l’animal peut être considéré comme relativement limité » (p. 5) – « Le groupe de travail estime que l’analyse qui a été conduite montre que le niveau de preuve de cancérogénicité chez l’animal et chez l’Homme peut être considéré comme relativement limité et ne permet pas de proposer un classement 1B dans le cadre de l’application des critères du règlement (CE) n° 1272/2008 » (p. 5). Nota : Le classement 1B du règlement européen CLP correspond au classement « cancérogène probable (groupe 2A) » du CIRC. |
| Réunion mixte de la FAO et de l’OMS sur les résidus de pesticides (JMPR, 16 mai 2016) [2] :
– « Le poids global de la preuve indique que l’administration de glyphosate et de ses produits de formulation à des doses aussi élevées que 2 000 milligrammes par kg de poids corporel par voie orale [...], n’a pas été associée à des effets génotoxiques dans une écrasante majorité des études menées chez les mammifères » (p. 2) – « Le JMPR a conclu qu’il est improbable que le glyphosate soit génotoxique aux expositions alimentaires anticipées » (p. 2) – « Compte tenu de l’absence de potentiel cancérogène chez les rongeurs à des doses pertinentes pour l’Homme et de l’absence de génotoxicité par voie orale chez les mammifères et compte tenu des preuves épidémiologiques d’expositions professionnelles, le JMPR a conclu que le glyphosate est peu susceptible de présenter un risque cancérogène pour l’Homme à travers le régime alimentaire » (p. 2). |
| Autorité de protection de l’environnement de Nouvelle Zélande (NZ EPA, août 2016) [8] :
– « En raison de l’incohérence des résultats des études sur l’exposition au glyphosate et le lymphome non-hodgkinien et de l’absence d’association dans l’étude la plus vaste et la plus robuste, il n’y a aucune preuve convaincante d’une association entre l’exposition au glyphosate et le développement du cancer chez les humains » (p. 1) – « Toutes les études réalisées selon les lignes directrices d’essais internationalement reconnues n’ont pas trouvé de preuve d’un effet génotoxique du glyphosate » (p. 2) – « Il a été conclu que le poids de la preuve indique que le glyphosate n’est pas génotoxique » (p. 2) – « Il est conclu que le poids global de la preuve indique que le glyphosate n’est pas cancérogène » (p. 15) – « La conclusion générale est que – se basant sur une approche fondée sur le poids de la preuve, tenant compte de la qualité et de la fiabilité des données disponibles – il est improbable que le glyphosate soit génotoxique ou cancérogène pour l’Homme et il ne mérite pas d’être classé comme cancérogène ou mutagène selon la loi HSNO » (p. 16). |
| Agence américaine de protection de l’environnement (US EPA, 12 septembre 2016) [9] :
– « En se basant sur le poids de la preuve, l’agence a déterminé que les tumeurs observées dans les études de cancérogénicité chez le rat et la souris pour le glyphosate ne sont pas considérées comme liées au traitement » (p. 96) – « Les données de génotoxicité sont hautement reproductibles et cohérentes avec une démonstration claire que le glyphosate n’a pas de mécanisme d’action mutagénique » (p. 136) – « Le soutien le plus fort appuie la mention “non susceptible d’être cancérogène pour l’Homme” à des doses pertinentes pour l’évaluation des risques pour la santé humaine » (p. 140). |
| Autorité australienne des pesticides et des médicaments vétérinaires (APVMA, septembre 2016) [10,11,12] :
– « L’APVMA a conclu que le glyphosate ne présente pas de risque cancérogène chez l’humain » [10] – « L’exposition au glyphosate ne présente pas de risque cancérogène ou génotoxique pour l’Homme » ([11] p. 9) – « Le poids des preuves indique que le glyphosate n’est pas carcinogène pour les animaux de laboratoire et n’est pas génotoxique » ([12], p. 41). |
| Commission japonaise de sécurité des aliments (FSCJ, 30 septembre 2016) [13] :
– « Le glyphosate ne présente ni neurotoxicité, ni cancérogénicité, ni toxicité pour la reproduction, ni teratogénicité, ni génotoxicité ». |
| Agence européenne des produits chimiques (ECHA, 15 mars 2017) [5] :
– « Le comité d’évaluation des risques n’a pas trouvé de preuves suffisantes pour soutenir un mécanisme d’action génotoxique du glyphosate et a conclu, d’après les données épidémiologiques et les données d’études à long terme chez le rat et la souris, qu’aucune classification de danger pour la cancérogénicité n’est justifiée pour le glyphosate selon les critères CLP » (p 6). |
| Agence canadienne de réglementation de la lutte antiparasitaire (ARLA, 28 avril 2017) [14] :
– « Le glyphosate n’est pas génotoxique et il est peu probable qu’il présente un risque de cancer pour les humains » (p. 1) – « L’ARLA n’a relevé aucun potentiel génotoxique pour le principe actif qu’est l’acide glyphosate » (p. 20). |
Analyse des études de génotoxicité
Pour le CIRC, la génotoxicité du glyphosate est établie : il indique disposer de « preuves solides ». Pour toutes les autres agences, le glyphosate ne présente pas de potentiel génotoxique. L’Anses parle de niveau de preuve « relativement limité » mais passe la main à l’ECHA pour une évaluation plus précise, en indiquant que le point le plus préoccupant soulevé par le CIRC à ce sujet « mériterait d’être évalué avec la plus grande attention dans le cadre des discussions sur le classement de la substance active qui auront lieu sous la responsabilité de l’ECHA » [7]. L’ECHA a procédé à cette évaluation et « n’a pas trouvé de preuves suffisantes pour soutenir un mécanisme d’action génotoxique du glyphosate » [5]. L’EFSA et le JMPR jugent « improbable » la génotoxicité du glyphosate, les autres agences sont encore plus catégoriques. Le BfR allemand indique que « le glyphosate n’induit pas de mutations in vivo », l’EPA néo-zélandaise que « le glyphosate n’est pas génotoxique », l’EPA américaine qu’il « n’a pas de mécanisme d’action mutagénique », l’APVMA qu’il « n’est pas génotoxique », la FSCJ qu’il ne « présente pas de génotoxicité », l’ARLA qu’il « n’est pas génotoxique ».
Il existe plusieurs centaines d’études scientifiques documentant le potentiel génotoxique du glyphosate. La sélection des études jugées pertinentes est donc un point crucial de l’évaluation. Dans ce domaine, le CIRC se démarque des autres agences. Pour l’évaluation de la génotoxicité, le CIRC a retenu une centaine d’études, c’est-à-dire à peu près le même nombre que les autres agences ayant mené cette évaluation. Mais le CIRC a retenu un grand nombre d’études sur non-mammifères alors que toutes les autres agences ayant mené cette évaluation ont privilégié les études sur mammifères. Le CIRC a par exemple retenu 54 études de génotoxicité in vivo sur les organismes suivants : poissons (26 études), huîtres (2), insectes (3), caïmans (4), grenouilles (3), plantes (9), palourde (1), escargots (1), vers (4) et moules (1). Pourtant, l’objectif de la monographie du CIRC est bien l’extrapolation à l’Homme et il est bien établi que les modèles animaux les plus pertinents dans ce but sont les mammifères. L’US EPA explique, en accord avec des observations similaires du BfR et de l’ECHA, que « les études menées sur des espèces non-mammifères ont été exclues parce qu’elles ne sont pas pertinentes pour documenter un risque génotoxique chez les humains ». Bref, selon toutes les agences à l’exception du CIRC, il est fragile d’extrapoler à l’Homme des résultats trouvés sur des classes animales non-mammifères lorsqu’ils ne sont pas reproduits sur des mammifères.
Le CIRC a aussi retenu, dans son analyse de génotoxicité, 76 études testant non pas du glyphosate seul, mais des formulations herbicides contenant du glyphosate associé à des coformulants. Or, le BfR fait remarquer que certains coformulants seuls, notamment des surfactants, sont clairement plus toxiques que le glyphosate. Le CIRC cite d’ailleurs aussi plusieurs études démontrant que des formulations sont plus toxiques que le glyphosate seul. D’ailleurs, en juin 2016, en France, l’Anses a annulé l’autorisation de tous les produits herbicides contenant du glyphosate associé à des surfactants particuliers, les POE-tallowamines, ce qui a entraîné le retrait de la vente de 132 produits herbicides [15]. La présence des coformulants constitue donc un facteur de confusion biaisant l’évaluation lorsqu’on cherche à évaluer l’effet du glyphosate lui-même. Pour cette raison, à l’exception du CIRC, les agences se sont basées sur les études avec glyphosate seul pour estimer sa génotoxicité.
Le choix des études est donc un facteur explicatif de la différence d’évaluation entre le CIRC et les autres agences. L’agence néo-zélandaise résume cet aspect en indiquant que « toutes les études réalisées selon les lignes directrices d’essais internationalement reconnues n’ont pas trouvé de preuve d’un effet génotoxique du glyphosate ». Il est difficile de dire quelle aurait été la conclusion du CIRC s’il s’était basé sur les mêmes études que les autres agences, et réciproquement. La conclusion de l’US EPA selon laquelle les « données de génotoxicité sont hautement reproductibles et cohérentes avec une démonstration claire que le glyphosate n’a pas de mécanisme d’action mutagénique » tranche radicalement avec celle du CIRC qui indique au contraire qu’il « existe des preuves solides que le glyphosate cause une génotoxicité ».
Mais, attention, il ne faut pas accorder au critère de génotoxicité plus d’importance qu’il n’en a dans l’évaluation du caractère cancérogène du glyphosate. Les critères d’évaluation du CIRC mentionnent que pour justifier un classement « cancérogène probable » (groupe 2A) pour l’Homme, il faut impérativement disposer de « preuves suffisantes » de cancérogénicité chez l’animal, qui ne peuvent être apportées que par les études de cancérogenèse de long terme et nullement par les études de génotoxicité [16]. En complément, les « preuves limitées » de cancérogenèse chez l’Homme, fondées sur les études épidémiologiques, sont nécessaires pour justifier la classification 2A. Ainsi, les éléments de preuve de génotoxicité ne font que renforcer l’évaluation de cancérogenèse mais ne la justifient nullement.
Analyse des études de cancérogénèse animale
Le CIRC affirme disposer de « preuves suffisantes de cancérogénicité du glyphosate sur les animaux de laboratoire » tandis que l’agence européenne EFSA indique « qu’aucune preuve de cancérogénicité n’a été observée chez le rat ou la souris ». L’agence française Anses retient un niveau de preuve « relativement limité ». L’agence conjointe de l’OMS et de la FAO (JMPR), évoque « l’absence de potentiel cancérogène chez les rongeurs à des doses pertinentes pour l’Homme ». L’agence américaine US EPA considère que les tumeurs observées dans les études de cancérogenèse animales ne sont pas liées au glyphosate. L’agence australienne APVMA conclut que « le poids des preuves indique que le glyphosate n’est pas carcinogène pour les animaux de laboratoire ». L’unanimité apparente contre l’avis du CIRC sur les résultats des études de cancérogénèse animale doit être expliquée.
Il existe des dizaines d’études de cancérogenèse animale de long terme pour le glyphosate. Après filtrage des études peu pertinentes ou jugées trop faibles par toutes les agences (y compris le CIRC), il reste 19 études retenues par au moins une agence. Le CIRC en a retenu huit et s’est fixé une ligne de conduite consistant à ne jamais évaluer des données qui ne sont pas disponibles publiquement, même s’il peut lui-même y accéder. Cela dit, il ne s’interdit pas de tenir compte indirectement des résultats des études non publiées, lorsque suffisamment de données ont été rendues publiques dans des articles de synthèse ou dans des avis des autres agences sanitaires. Les études non publiées sont des études réglementaires exigées par les agences sanitaires auprès des industriels qui souhaitent faire autoriser leur produit.
Pour quatre études sur les huit qu’il a retenues, le CIRC conclut à l’absence d’indice de cancérogénicité du glyphosate chez l’animal. Les quatre études de cancérogénèse animales restantes, dans lesquelles le CIRC trouve des indices de cancérogénicité du glyphosate (non significatifs pour deux études [17,18] mais significatifs pour deux autres [19,20], au seuil 5%), sont des études réglementaires financées par les industriels (Monsanto ou Cheminova), dont certains résultats ont été rendus publics dans des publications de l’US EPA et du JMPR. La plus récente de ces quatre études date de 1993, il y a 24 ans. Depuis, elles ont été étudiées par les agences sanitaires du monde entier, sans qu’aucune n’en tire de preuves suffisantes de cancérogénicité du glyphosate. En 2015, soit 22 ans après la plus récente, le CIRC considère que ces études apportent, enfin, des « preuves suffisantes » de cancérogénicité du glyphosate pour les rats et les souris.
Parmi les agences ayant analysé ces quatre études, seul le CIRC met en cause le glyphosate. Toutes les autres ne voient que des aléas statistiques, sans signification biologique, justifiant leurs avis par une analyse du « poids des preuves » (voir encadré).
L’évaluation du poids des preuves
L’« évaluation du poids des preuves » (Weight of Evidence en anglais) est, comme le rappelle l’Anses[24] « la méthodologie permettant d’évaluer la pertinence et la qualité des données, puis de combiner des données hétérogènes ». Cependant, toutes les agences n’ont pas les mêmes guides méthodologiques et systèmes de classification. Et, comme le souligne l’Anses, ceci peut contribuer à expliquer « les divergences entre les conclusions apportées par différents organismes sur la toxicité ou sur le risque lié à l’exposition à diverses substances (par exemple, entre l’EFSA et l’IARC sur le glyphosate ; entre l’EFSA et l’Anses sur le Bisphénol A) ».
Ainsi, pour le glyphosate, les divergences d’interprétation des données de cancérogénicité animale entre le CIRC d’une part, et l’ensemble des autres agences d’autre part, s’explique par deux éléments principaux :
- une différence d’interprétation sur deux études particulières [19,20] où le CIRC retient l’hypothèse de la responsabilité du glyphosate dans l’apparition de tumeurs chez des rats et des souris ;
- l’appréciation du poids des preuves différentes qui conduisent le CIRC à accorder une importante prépondérante à ces études par rapport à toutes les autres études rassurantes.
Sur les deux études divergentes
À propos de l’étude [19] (Monsanto 1990), le CIRC retient une incidence statistiquement significative de tumeurs bénignes du pancréas chez les mâles traités à la plus faible et à la plus forte dose. Il note aussi une tendance positive statistiquement significative de l’incidence de tumeurs bénignes du foie chez les mâles et de tumeurs bénignes de la thyroïde chez les femelles. Ces éléments avaient été mis en avant initialement par l’US EPA qui a confirmé « sur la base du poids de la preuve », ne pas considérer que ces tumeurs sont liées au traitement, comme les autres agences.
À propos de l’étude [20] (Monsanto 1983), le CIRC note une « augmentation significative de l’incidence de tumeurs rares, avec une tendance liée à la dose, qui pourrait être attribuée au glyphosate ». C’est l’US EPA qui, dans un avis publié en 1985, avait le premier signalé ces tumeurs rénales rares mises en avant en 2015 par le CIRC. Mais, à nouveau, l’US EPA a conclu que, suite à « un examen approfondi de toutes les coupes rénales », à des « évaluations pathologiques et statistiques supplémentaires » et « sur la base du poids de la preuve pour cette étude », les tumeurs rénales ne sont pas liées au traitement, rejoignant l’avis des autres agences.
Sur l’analyse globale du poids des preuves
Chacune de 19 études de cancérogénèse animales jugées pertinentes comporte quatre groupes d’animaux de chaque sexe (comptant au moins 50 individus chacun), incluant, pour chaque sexe, un groupe témoin et trois groupes traités à différentes doses. Chaque étude donne donc lieu à six comparaisons entre un groupe traité et son groupe témoin correspondant auquel s’ajoute un test de tendance par sexe, pour chaque type de tumeur considéré. Il faut donc s’attendre à quelques comparaisons statistiquement significatives par le simple jeu du hasard (au seuil 5%). Les agences d’évaluation des risques relativisent donc les quelques résultats mis en avant par le CIRC en évoquant le « poids de la preuve ». Les lignes directrices d’évaluation du CIRC, expliquent que pour déclarer les « preuves suffisantes » de cancérogénicité chez l’animal, il suffit que deux études indépendantes aient trouvé, pour un sexe, des associations jugées pertinentes entre l’exposition à l’agent et l’incidence d’un cancer, ou bien qu’une seule étude bien conduite ait trouvé, pour les deux sexes, une incidence augmentée de tumeurs en lien avec l’exposition à l’agent. La probabilité de satisfaire ces conditions s’accroît avec le nombre d’études pertinentes disponibles.
En outre, concernant l’étude [20] (Monsanto 1983), la plus significative des deux études mises en avant par le CIRC, la tendance positive observée est due à trois cas de tumeurs rénales rares dans le groupe de cinquante souris mâles exposées à la dose la plus élevée de glyphosate, qui était de cinq grammes par kilo de poids corporel et par jour. Selon des recommandations mondialement acceptées, la dose de glyphosate ne doit pas dépasser 1 g/kg/jour dans les études de cancérogénèse sur des souris. Au-delà, l’estomac des animaux est attaqué par l’acidité du produit et cela perturbe l’évaluation de cancérogénèse. D’ailleurs, le CIRC note dans son analyse la « diminution conséquente du poids corporel chez les souris mâles et femelles à la dose la plus élevée ». Un rapide calcul montre que pour un homme de 70 kg, une dose de 5 g/kg/jour correspond à une consommation quotidienne de 350 grammes de glyphosate. Donnez donc un grand bol de glyphosate chaque matin au petit déjeuner à cinquante hommes pendant toute leur vie et vous observerez, en fin de vie, trois cas de tumeurs rénales rares, sous l’hypothèse que les tumeurs observées étaient bien liées au seul glyphosate 2. Une telle exposition au glyphosate ne correspond à aucun scénario réaliste d’exposition humaine. Par conséquent, ce résultat pris en compte par le CIRC, à juste titre compte tenu de sa mission d’identification de danger indépendamment du niveau d’exposition, n’a pas de valeur pour l’évaluation des risques pour l’Homme et doit donc être, à juste titre aussi, ignoré par les agences d’évaluation des risques.
Finalement, l’appréciation précautionneuse du poids des preuves par le CIRC, découlant de ses lignes directrices d’évaluation, et l’indifférence au caractère réaliste de la dose que suppose une évaluation de danger et non de risque, ont conduit le groupe de travail à retenir les « preuves suffisantes » de cancérogénicité du glyphosate pour l’animal, en décalage avec toutes les autres agences. Par suite, c’est cette conclusion de « preuves suffisantes » de cancérogénicité pour l’animal qui constitue l’argument principal en faveur du classement « cancérogène probable » (groupe 2A) du glyphosate pour l’Homme. Néanmoins, pour prétendre au classement 2A, les lignes directrices du CIRC prévoient que doivent aussi être retenues les « preuves limitées » de cancérogénicité pour l’Homme dans les études épidémiologiques.
Analyse des études épidémiologiques chez l’Homme
Pour évaluer la cancérogénicité pour l’Homme, les agences se sont toutes appuyées sur les mêmes études épidémiologiques. Elles en ont considéré 26 : cinq études de cohorte et 21 études cas-témoins. Aucune des cinq études de cohorte n’a identifié de potentiel cancérogène des herbicides à base de glyphosate, y compris pour le lymphome non-hodgkinien (LNH). Sur les 21 études cas-témoins, 17 n’ont pas montré d’association positive entre utilisation d’herbicide à base de glyphosate et cancer. Les quatre études cas-témoins restantes ont montré des associations positives entre exposition aux herbicides à base de glyphosate et le LNH chez des agriculteurs. C’est sur ces quatre études cas-témoins que s’appuie le CIRC pour soutenir qu’il existe des « preuves limitées » de cancérogénicité pour l’Homme pour le LNH.
Voici les arguments les plus saillants que les autres agences ont opposé à l’analyse du CIRC :
• L’US EPA a montré que certaines associations positives entre exposition au glyphosate et le LNH, mises en avant par le CIRC dans les quatre études, disparaissent lorsqu’on tient compte de l’exposition des agriculteurs à d’autres herbicides, notamment les herbicides phénoxy, qui sont connus pour être davantage à risque vis-à-vis du LNH que le glyphosate. Finalement, les seules associations significatives restantes sont celles pour lesquelles la correction n’a pas pu être effectuée, faute d’information suffisante sur l’utilisation d’autres pesticides. Ceci doit inciter à la prudence dans l’interprétation de ces résultats.
• Les études cas-témoins sont particulièrement sujettes au biais de rappel car l’évaluation de l’exposition au glyphosate passe par des questionnaires a posteriori, nécessitant que les personnes interrogées, parfois des proches d’une personne décédée ou malade, se souviennent de l’exposition du « cas » au produit, sur des décennies. Outre l’imprécision flagrante de ce type d’évaluation, il est bien établi que les personnes touchées par une maladie ont tendance à apprécier leur exposition à un produit « suspect » à un niveau plus élevé que les témoins. Ce biais peut expliquer que quelques études cas-témoins montrent des associations positives qu’aucune des études de cohorte, moins sujettes à ce biais, ne montre.
• À l’exception du CIRC, les agences considèrent que le « poids de la preuve » apporté par les cinq études épidémiologiques de cohorte ne montrant aucun lien entre l’exposition aux herbicides à base de glyphosate et cancer l’emporte sur les quelques associations positives – suspectes de biais – trouvées dans des études cas-témoins. En particulier, elles désignent toutes l’étude basée sur une cohorte de 54 000 agriculteurs américains (cohorte AHS) [22], comme étant la plus puissante. L’agence néo-zélandaise résume ces considérations en indiquant qu’il est « important de considérer l’ensemble des données disponibles plutôt que de souligner seulement les quelques études de cas-témoins qui ont identifié une association statistiquement significative entre l’utilisation du glyphosate et le lymphome non-hodgkinien » et que « étant donné l’absence de confirmation du petit nombre de résultats positifs d’études cas-témoins dans l’étude de cohorte la plus puissante, le soutien épidémiologique à la conclusion “preuves limitées” chez les humains n’est pas convaincant » [8].
Finalement, la position du CIRC sur les études épidémiologiques est isolée, mais peut s’expliquer par la nature précautionneuse de ses évaluations. Les lignes directrices d’évaluation en vigueur au CIRC indiquent que les « preuves limitées » de cancérogénicité pour l’Homme doivent être retenues par le groupe de travail dès qu’« une association positive a été observée entre l’exposition à l’agent et le cancer, pour laquelle une interprétation causale est considérée crédible par le groupe de travail, mais le hasard, le biais ou la confusion ne peuvent être écartés avec une confiance raisonnable » [21]. Cette description peu contraignante s’adapte à de nombreuses situations et peut certainement s’appliquer ici, comme le remarque le BfR allemand.
Glyphosate et cancer – conclusion
Au terme de notre analyse, nous arrivons à la conclusion qu’après plus de quarante ans de recherche scientifique active, aucun indice convaincant de cancérogénicité du glyphosate pour l’Homme ne s’est manifesté à des doses compatibles avec une exposition humaine réaliste. Toutes les agences sanitaires ayant mené une réévaluation du potentiel cancérogène du glyphosate suite à l’avis du CIRC l’ont à nouveau déclaré non cancérogène. Notamment, l’ECHA, dont les classifications de danger ont valeur réglementaire en Europe.
En outre, une nouvelle étude épidémiologique d’envergure vient d’être publiée dans la revue scientifique Journal of the National Cancer Institute [23]. Il s’agit d’une vaste étude de cohorte prospective, ayant suivi 54 251 agriculteurs américains sur plus de vingt ans. Cette étude ne trouve pas de lien entre exposition aux herbicides à base de glyphosate et l’apparition de cancer, notamment de lymphome non-hodgkinien. Les auteurs concluent : « Dans cette vaste étude de cohorte prospective, aucune association n’apparaît entre le glyphosate et les tumeurs solides ou lymphoïdes malignes, y compris le lymphome non-hodgkinien et ses sous-types ». Cette nouvelle étude est une réactualisation de l’étude de 2005 [22] qui était déjà considérée comme assez solide par les agences sanitaires, bien que ne portant à l’époque que sur sept années de suivi. Avec un suivi de plus de vingt ans de cette vaste cohorte d’agriculteurs, les conclusions rassurantes des agences sanitaires se trouvent donc corroborées.
L’avis du CIRC ne semble pas s’intégrer dans ce tableau rassurant. Ses fondements précautionneux, donnant plus de poids aux indices à charge qu’aux indices à décharge, interrogent. Ils semblent adaptés pour détecter au plus tôt le danger cancérogène d’un produit nouveau ou peu étudié, mais peu pertinents pour évaluer le danger d’un produit ancien et longuement étudié bénéficiant d’un vaste corpus d’études scientifiques. De fait, au moment où le CIRC a émis son avis sur le glyphosate en 2015, la synthèse de la masse d’études scientifiques disponibles permettait déjà de soutenir que le glyphosate ne posait pas de risque cancérogène en pratique, comme l’attestaient les avis unanimes des agences d’évaluation des risques du monde entier.
L’agitation médiatique évoquée au début de notre article provient en partie de l’incompréhension par le public de la portée réelle des avis du CIRC. La différence fondamentale entre identification d’un danger et évaluation d’un risque n’est pas comprise. Le rôle du CIRC, intervenant en amont du processus d’évaluation des risques, n’est pas compris. Ces incompréhensions conduisent à l’instrumentalisation sans limite des avis du CIRC, sans considération de leur valeur pratique limitée, poussant même des gouvernements à invoquer l’application du principe de précaution sans tenir compte des avis des agences publiques d’évaluation des risques.
En appliquant les mêmes méthodes d’analyses, le CIRC a classé le jambon dans le groupe 1 « cancérogène certain pour l’Homme » 3, classement supérieur à celui du glyphosate, dans lequel figurent aussi l’amiante, l’arsenic et le plutonium.
Non cancérogène, le glyphosate serait-il pour autant sans risque ?

L’évaluation des risques du glyphosate ne saurait se résumer à son potentiel cancérogène. L’ECHA rappelle que le glyphosate ne présente pas de danger pour la reproduction mais peut provoquer des lésions oculaires graves et qu’il est toxique pour les organismes aquatiques avec des effets à long terme. Sur la base de ces évaluations de dangers, les agences d’évaluation des risques recommandent de porter des lunettes lors de l’application et de ne pas pulvériser d’herbicide à base de glyphosate à moins de quelques mètres d’un cours d’eau. Moyennant ces précautions d’usage, elles affirment unanimement que l’utilisation du glyphosate ne présente pas de risque préoccupant pour la santé et l’environnement, comme résumé par l’agence canadienne (ARLA) en français [14] :
– « Le glyphosate n’est pas génotoxique et il est peu probable qu’il présente un risque de cancer pour les humains. »
– « L’exposition par le régime alimentaire (eau potable et aliments) associée à l’utilisation du glyphosate ne devrait pas présenter de risque pour la santé humaine. »
– « Les risques professionnels et résidentiels associés à l’utilisation du glyphosate ne sont pas préoccupants, sous réserve que les modes d’emploi révisés figurant sur les étiquettes soient respectés. »
– « Les produits contenant du glyphosate ne devraient pas poser de risques préoccupants pour l’environnement lorsqu’ils sont utilisés conformément au mode d’emploi proposé sur l’étiquette. »
Mais n’en concluez pas que vous pouvez utiliser cet acide dans la préparation du biberon d’un nouveau-né ! En ce qui concerne les risques sanitaires liés aux résidus de glyphosate dans les aliments, la dernière étude de l’EFSA [25] montre qu’un consommateur européen dont la consommation de denrées alimentaires correspondrait aux repères maximum considérés devrait multiplier plusieurs milliers de fois sa consommation alimentaire de produits contaminés pour atteindre la dose maximale quotidienne de glyphosate jugée sans effet adverse sur sa santé sur toute sa vie.
Enfin, une récente étude de l’EFSA [26] conclut « sur la base de l’ensemble des données toxicologiques disponibles » que le glyphosate n’a pas de pouvoir perturbateur endocrinien.
Les débats sont d’autre part très animés au sein des institutions européennes pour déterminer si les réglementations relatives à la perturbation endocrinienne des produits devraient se fonder sur une évaluation de danger, comparable à l’évaluation de la cancérogénicité des produits par le CIRC, ou sur une évaluation du risque comparable aux évaluations pratiquées par les agences d’évaluation des risques du monde entier.
0 | “Les Monographies du CIRC démystifiées : retour sur six idées fausses”, 15 juin 2016 sur iarc.fr
1 | IARC, “Monography on Glyphosate, in Some Organophosphate Insecticides and Herbicides”, IARC Monographs on the Evaluation of Carcinogenic Risks to Humans, 2017, 112:321-412. Sur monographs.iarc.fr
2 | “Joint FAO WHO meeting on pesticide residues – Summary report”, 16 mai 2016. Sur who.int
3 | “EFSA explains the carcinogenicity assessment of glyphosate”, 12 novembre 2015. Sur efsa.europa.eu
4 | EFSA, “Conclusion on the peer review of the pesticide risk assessment of the active substance glyphosate”, EFSA Journal, 2015, 13:4302. Sur efsa.europa.eu
5 |“Explanatory note on an opinion proposing harmonised classification and labelling at EU level of glyphosate (ISO) ; N-(phosphonomethyl)glycine”, ECHA, 15 mars 2017. Sur echa.europa.eu
6 | “Glyphosate Renewal Assessment Report – Assessment of IARC Monographs Volume 112 (2015) : Glyphosate”, 31 août 2015. Sur gmwatch.org
7 | “Avis de l’Agence nationale de sécurité sanitaire de l’alimentation, de l’environnement et du travail relatif à la saisine glyphosate n° 2015-SA-0093”, 9 février 2016. Sur anses.fr
8 |“Review of the Evidence Relating to Glyphosate and Carcinogenicity” Prepared for the Environmental Protection Authority by Dr Wayne Temple, août 2016. Sur www.epa.govt.nz
9 | “Glyphosate Issue Paper : Evaluation of Carcinogenic Potential EPA’s Office of Pesticide Programs”, 12 septembre 2016. Sur epa.gov
10 l Page “glyphosate” du site de l’Autorité australienne des pesticides et des médicaments vétérinaires du gouvernement australien. Sur apvma.gov.au
11 |“Final regulatory position : Consideration of the evidence for a formal reconsideration of glyphosate”, Autorité australienne des pesticides et des médicaments vétérinaires du gouvernement australien, mars 2017. Sur apvma.gov.au
12 | “Review of IARC Monograph 112 (Glyphosate) : Tier 2”, Autorité australienne des pesticides et des médicaments vétérinaires du gouvernement australien, mars 2016. Sur apvma.gov.au
13 | Food Safety / Volume 4 (2016) Issue 3 / Risk Assessment Report : Pesticides / Glyphosate /Food Safety Commission of Japan
14 | « Décision de réévaluation RVD2017-01 Glyphosate », Agence de réglementation de la lutte antiparasitaire de Santé Canada, 28 avril 2017. Sur publications.gc.ca
15 | « Retrait des produits phytopharmaceutiques associant en coformulation glyphosate et POE-Tallowamine du marché français », Anses, 20 juin 2016. Sur anses.fr
16 | « Classification des substances cancérogènes par le CIRC », 28 février 2017. Sur cancer-environnement.fr
17 | Lankas GR, Hogan GK, "A lifetime feeding study of glyphosate (Roundup Technical) in rats", Rapport non publié, 1981, par Bio/dynamics Inc. pour Monsanto, Report 77-2062, MRID 00093879, TOX2000-595, TOX2000-1997.
18 | Atkinson C, Martin T, Hudson P, Robb D, “Glyphosate : 104 week dietary carcinogenicity study in mice”, Rapport non publié, 1993, par Inveresk Research International pour Cheminova, IRI Project 438618, MRID 49631702, TOX9552382.
19 | Stout LD, Ruecker PA, “Chronic study of glyphosate administered in feed to albino rats”, Rapport non publié, 1990, pour Monsanto, MRID 41643801, TOX9300244.
20 | Knezevich AL, Hogan GK, “A chronic feeding study of glyphosate in mice”, Rapport non publié, 1983, par Bio/Dynamics Inc. pour Monsanto, Report 77-2011, MRID 00130406, TOX9552381.
21 | “Preamble to the IARC monographs – Scientific review and evaluation”. Sur monographs.iarc.fr
22 | De Roos A et al., “Cancer incidence among glyphosate-exposed pesticide applicators in the Agricultural Health Study”, Environ Health Perspect, 2005, 113:49-54.
23 | Gabriella Andreotti et al., “Glyphosate Use and Cancer Incidence in the Agricultural Health Study”, Journal of the National Cancer Institute, 2017.
24 | « Évaluation du poids des preuves : revue critique de la littérature et recommandations à l’étape d’identification des dangers », avis de l’Anses, juillet 2016.
25 | “The 2015 European Union report on pesticide residues in food” European Food Safety Authority, approuvé le 7 avril 2015.
26 | “Peer review of the pesticide risk assessment of the potential endocrine disrupting properties of glyphosate”, European Food Safety Authority, 17 août 2017. Sur efsa.europa.eu
1 Toutes les traductions depuis l’anglais sont de l’auteur du présent article.
2 Ce qui est douteux car les femelles traitées à la même dose n’ont pas été atteintes de tumeurs rénales dans cette étude et le résultat n’a pas été répliqué dans d’autres études.
3 Précisément, toutes les "viandes transformées" ont été classées "cancérogène certain pour l’homme", ce qui inclut toutes les charcuteries.
Publié dans le n° 323 de la revue
Partager cet article
L' auteur

Hervé Le Bars
Hervé Le Bars est membre du comité de rédaction de la revue de l’Afis Science & pseudo-sciences. Ingénieur de (...)
Plus d'informationsPesticides

Le glyphosate est-il cancérogène ?
Le 16 février 2018
Chronologie de l’« affaire » des pesticides SDHI
Le 23 septembre 2020Communiqués de l'AFIS

« Extinction Rebellion » tente d’interdire une conférence de l’Afis
Le 3 février 2023













![[Lyon - samedi 29 avril 2023] Pollution des Antilles au Chlordécone : Origines et conséquences](local/cache-gd2/8b/1668648b1d4cf123c90d8e3194fba0.jpg?1681553459)
![[Paris - jeudi 2 février 2023] Glyphosate - Santé, Environnement, Agronomie : Comment s'y retrouver ?](local/cache-gd2/b0/8778a383cc5b44b4c0c95cb1ccd51f.jpg?1681577057)