Dossier • Radioactivité : quels risques aux faibles doses ?
Du nouveau sur l’effet des faibles doses de rayonnement ?
Publié en ligne le 22 mai 2016 - Nucléaire -Un rayonnement ionisant pénétrant dans une cellule peut avoir quatre types d’effets : ou bien rien ne se passe, ou bien d’éventuelles lésions de l’ADN sont réparées ad integrum, ou bien la cellule meurt à plus ou moins court terme, ou bien des mutations sont induites dans l’ADN. Si, du fait d’une irradiation intense, touchant une partie critique de l’organisme, de nombreuses cellules meurent, des troubles graves peuvent se déclencher chez l’individu irradié, pouvant aller jusqu’à la mort dans les quelques jours, semaines ou mois suivant l’irradiation. C’est ce qu’on appelle les effets déterministes des radiations. Pour des irradiations plus faibles, les éventuelles mutations induites dans l’ADN peuvent ou non induire des cancers. C’est le domaine des effets dits probabilistes. C’est de ce domaine qu’il s’agit quand on parle de faibles doses, et c’est à lui que nous allons nous intéresser car c’est le seul qui importe lorsqu’il s’agit des effets sanitaires de l’industrie nucléaire pour le grand public.
La mesure des effets sanitaires des rayonnements ionisants
Les effets sanitaires des rayonnements dépendent en premier lieu de la quantité d’énergie reçue, appelée « dose absorbée ». On l’exprime en joule par kilogramme de matière vivante, c’est le gray (Gy). Le gray correspond à une forte irradiation. Les débits de doses que nous recevons de la radioactivité naturelle sont de l’ordre de quelques milligray (mGy) par an, de 2,5 à 100 mGy/an selon les endroits du globe. Les effets sanitaires dépendent aussi de la nature des rayonnements : par exemple, les rayons alpha sont vingt fois plus « efficaces » (pour entraîner un cancer) que les rayons gamma ou bêta. Ils dépendent aussi de la nature des organes irradiés. La « dose efficace » est supposée mesurer le risque sanitaire des radiations et est exprimée en sievert (Sv). Pour une irradiation homogène de tout l’organisme, par exemple par des rayons X ou gamma, la dose absorbée (en gray) et la dose efficace (en sieverts) sont égales. Il n’en est pas de même quand l’irradiation est inhomogène, comme c’est le plus souvent le cas lors de procédures médicales (diagnostiques ou thérapeutiques) ou de contamination par des produits radioactifs.

La quantification la plus utilisée du risque cancérigène des radiations est le Risque Relatif (RR) égal au rapport du nombre de cancers observés dans une population irradiée à celui qu’on observerait dans la même population en absence d’irradiation. Ainsi, un risque relatif de 2 signifie que les sujets exposés ont un risque de cancer 2 fois supérieur à celui des sujets non exposés. Un risque relatif de 1 signifie l’absence d’impact sur le nombre de cancers.
On utilise également l’Excès de Risque Relatif ERR : ERR= RR-1. C’est la proportion de cancers « en plus » créés par l’irradiation. Ainsi, pour un RR=1 on trouve logiquement un ERR égal à 0 (pas de cancer en plus).
Les faibles doses
La très grande majorité des irradiations « non naturelles », qu’il s’agisse des travailleurs du nucléaire, des chercheurs, des personnels de santé (radiologues, dentistes, vétérinaires) ou de la population générale (procédures médicales diagnostiques, retombées des essais nucléaires, contaminations induites par les accidents nucléaires) sont de faibles doses, inférieures à 100 mSv. La question du risque des faibles doses, par définition inférieures à 100 mSv, est de ce fait essentielle en radioprotection. Ce risque n’est pas mis en évidence par les grandes études épidémiologiques, soit parce qu’il n’existe pas, soit parce qu’il est trop faible pour être détecté, noyé dans le bruit de fond du risque de cancer (qui touche, naturellement, 20 à 40 % de la population 1). Pour les besoins de la radioprotection, faute de mieux, on estime ce risque des faibles doses par extrapolation jusqu’à zéro du risque avéré des fortes doses (en considérant essentiellement le suivi des survivants des bombardements atomiques d’Hiroshima et Nagasaki). Le risque, dans cette estimation, suit une relation « Linéaire Sans Seuil » notée RLSS.
On fait donc l’hypothèse que toute dose, si faible soit-elle, entraîne un risque relatif et que, pour toute dose, l’excès de risque (ERR) est proportionnel à la dose D (soit ERR = kD). Cette relation est utilisée pour la réglementation. Pour les faibles doses, elle ne repose pas sur des bases scientifiques, notamment biologiques, ou sur l’expérimentation animale. Elle n’est pas légitime pour calculer le nombre de cancers supplémentaires créés par une irradiation très faible mais touchant un grand nombre de personnes 2. Son utilisation à des fins strictement réglementaires conduit à définir des seuils très largement protecteurs.
Un certain nombre de données expérimentales montrent que l’extrapolation linéaire jusqu’à zéro qu’utilise la RLSS ne correspond pas à la réalité et que les mécanismes de défense des cellules contre les rayonnements ne sont pas les mêmes pour les faibles et les fortes doses, et proportionnellement plus efficaces pour les faibles doses, ce qui invalide toute extrapolation.
Une remise en cause des effets des faibles doses ?
Dans ce contexte, la récente publication d’un article dans la revue médicale le Lancet [1]) qui décrit l’étude INWORKS sous le titre : « Ionising radiation and risk of death from leukaemia and lymphoma in radiation-monitored workers (INWORKS) : an international cohort study » a été très remarquée.
Les conclusions de l’étude sont les suivantes (traduction par nos soins) : « Des irradiations ont été cumulées à très faibles doses (en moyenne 1,1 mGy (milligray) par an). L’excès relatif de mortalité par leucémie (leucémie myéloïde chronique exclue) est de 2,96/Gy, essentiellement du fait d’une association entre la dose d’irradiation et la mortalité par leucémie myéloïde chronique (ERR de 10,45/Gy). »
Analyse détaillée
La liste des maladies étudiées dans l’étude INWORKS sont données dans le tableau 1.
| 1. Leucémie sauf CLL | 5. Leucémie lymphoïde chronique (CLL) |
| 2. Leucémie myéloïde chronique | 6. Myélome multiple |
| 3. Leucémie myéloïde aigüe | 7. Lymphome non Hodgkinien |
| 4. Leucémie lymphoblastique aigüe | 8. Lymphome Hodgkinien |
L’étude a été faite sur une cohorte de 308 297 travailleurs (actifs ou retraités) du nucléaire (France, UK, USA) qui avaient été équipés de moniteurs de radiation pendant leur carrière professionnelle. Cette cohorte a été suivie dans le temps pour obtenir au total une puissance d’étude de 8,2 millions de personne-ans (durée moyenne de suivi individuel de 26 ans). Il a été possible de classer la cohorte selon la dose de rayonnement reçue, comme indiqué sur le tableau 2.
| Gamme de dose (mGy) | 0-5 | 5-50 | 50-100 | 100-200 | 200-300 | >300 |
|---|---|---|---|---|---|---|
| Nombre de personnes x ans | 5 315 000 | 2 299 000 | 344 500 | 185 800 | 49 660 | 27 700 |
| Dose moyennes (mSv) | 1 | 17,2 | 70 | 138 | 241 | 407 |
| Nombre de décès | 1 183 | 583 | 144 | 95 | 31 | 22 |
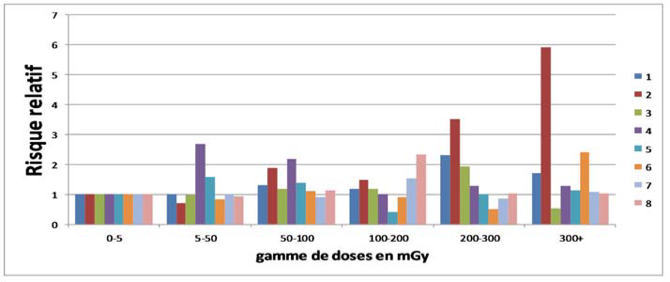
Dans l’article proprement dit, ne sont données que les valeurs du coefficient de corrélation linéaire entre la dose reçue et l’excès de risque relatif de cancer (ERR). L’article est complété par une annexe comportant des données numériques précises. Nous utilisons particulièrement la table A2 de cette annexe [2]. On peut en extraire un certain nombre de courbes qui montrent que, statistiquement, les conclusions de l’article INWORKS sont pour le moins discutables. La figure 1 montre que, pour les différents cas de cancers pris en compte au tableau 1, il est difficile de trouver un comportement commun. Une absence de corrélation entre dose et risque relatif n’est sûrement pas à exclure pour l’ensemble.
La publication du Lancet implique une analyse des résultats à l’aide d’une relation linéaire supposée valable aux très faibles doses et s’étendant au-delà de 300 mGy. Elle suppose que les réponses sanitaires à l’irradiation sont homogènes et linéaires, caractérisées par un seul paramètre. Or les incertitudes portent sur le domaine de doses inférieures à 100 mGy, ce qui nécessiterait un traitement spécifique des doses inférieures à 100 mGy. De plus, le fait que l’excès de risque relatif est une fonction croissante de la dose donne un poids croissant aux doses élevées dans les traitements statistiques, ce qui conduit à des valeurs du coefficient de proportionnalité largement déterminées par les excès de risque relatif aux hautes doses 3.
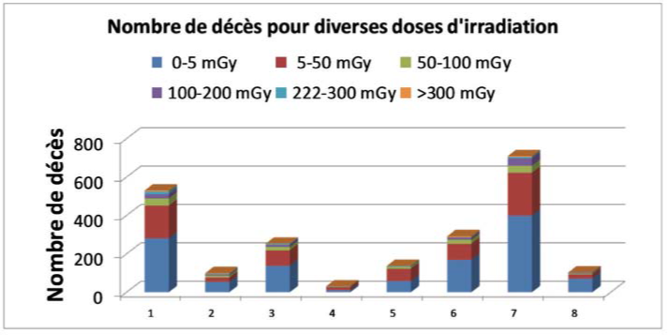
Les puissances statistiques (proportionnelles à la racine carrée du nombre de décès observés) sont assez différentes pour les 8 pathologies comme on peut le voir sur la figure 2. On remarque que les affections 2, 4 et 8, caractérisées par des Risques Relatifs (RR) élevés, correspondent à des mortalités particulièrement faibles.
En ne gardant que les 4 statistiques les plus élevées (1 : leucémie hors CLL, 3 : leucémie myéloïde aiguë, 6 : myélome multiple, 7 : lymphome non Hodgkinien), nous obtenons la figure 3.
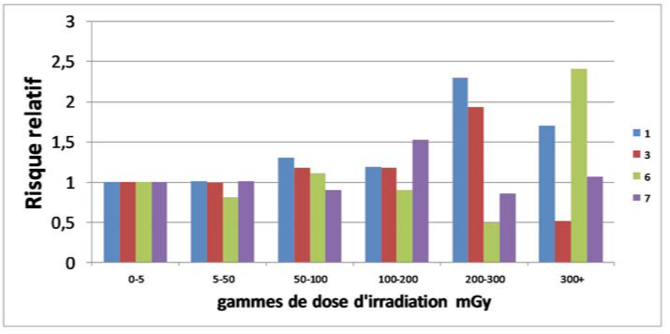
Sur la figure 3, on ne voit pas d’augmentation du risque relatif entre les intervalles 0-5 (valeur moyenne 1 mGy) et 5-50 mGy (valeur moyenne 17 mSv), qui correspondent au domaine des faibles doses, au contraire.
Une augmentation pourrait être présente entre les intervalles 5-50 et 50-100mGy, mais une indépendance du nombre de cancers par rapport à l’irradiation ne peut clairement pas être exclue, surtout si on prend en compte les irradiations dans l’intervalle 100-200 mGy.
Le tableau de l’annexe A de l’article INWORKS indique les valeurs des risques relatifs des 8 affections pour les gammes d’irradiation 5-50, 50-100, 100-200, 200-300 et supérieures à 300 mSv/an en référence avec les risques de la gamme 0-5 mSv/an 4. La figure 4 illustre ce comportement pour les leucémies myéloïdes chroniques, signalées dans l’article comme ayant des Risques Relatifs (RR) particulièrement élevés et croissant avec la dose.
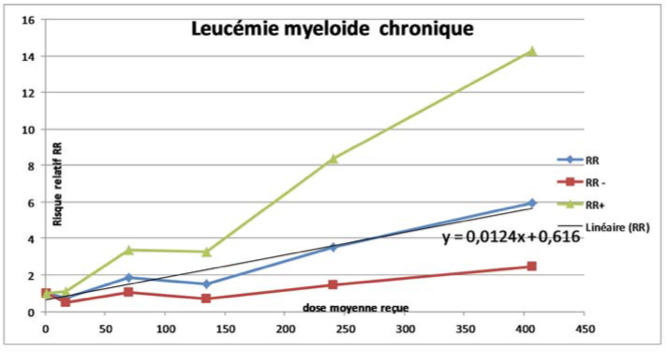
Au vu de la figure 4, on ne peut évidemment pas exclure une constance du risque pour des doses inférieures à 100 mGy, la relation linéaire ne s’affirmant qu’à partir de 150 mGy. Au-delà de cette valeur, l’excès de risque relatif est de l’ordre de 11 par Gy (compris entre 4 et 33 par Gy), en assez bon accord avec les valeurs données dans l’article. En limitant les doses prises en compte à 135 mSv, la valeur de l’excès de risque relatif est proche de 4 par Gy. Et une valeur nulle ne peut être exclue.
La figure 4 montre qu’il n’est pas légitime de traiter la corrélation entre doses et effets avec une unique et simple relation linéaire sans seuil. À tout le moins est-il nécessaire de tester l’hypothèse d’une indépendance du risque relatif de la dose dans le domaine des doses inférieures à 150 mGy.
Conclusion
Une analyse attentive de l’article « Ionising radiation and risk of death from leukaemia and lymphoma in radiation-monitored workers (INWORKS) : an international cohort study » paru dans The Lancet, et tout particulièrement des données numériques données dans son annexe ne confirme pas la validité d’une relation Linéaire Sans Seuil dans le domaine des doses inférieures à 100 mGy.
On peut regretter que les auteurs n’aient pas profité de l’importance de la cohorte étudiée pour approfondir la relation dose-effet pour les doses inférieures à 100 mGy. La figure 4 est une forte indication d’un comportement différent pour les doses inférieures à 150 mGy et celles supérieures à cette valeur. Par ailleurs, la figure 1 montre que les différentes pathologies sélectionnées semblent très loin d’être justifiables d’une approche commune. Il serait intéressant de reprendre cette étude sans a priori, en essayant de confirmer et comprendre les divers comportements observés.

Créé en 2001, l’IRSN est placé sous la tutelle conjointe des ministres en charge de l’Environnement, de l’Industrie, de la Santé, de la Recherche et de la Défense. Il est notamment chargé de fournir un appui technique aux services de l’État en charge du contrôle des activités nucléaires et de l’intervention publique en cas d’urgence, dans le domaine civil comme dans celui de la défense (sûreté, sécurité, non-prolifération, radioprotection), de mener pour le compte de l’État la surveillance radiologique du territoire et des personnes exposées aux rayonnements ionisants, et de conduire les recherches nécessaires à l’amélioration permanente de la sûreté nucléaire et de la protection des personnes et de l’environnement vis-à-vis des risques radiologiques. En 2006, la loi relative à la transparence et à la sécurité en matière nucléaire institue l’Autorité de sûreté nucléaire (ASN), dotée du statut d’autorité administrative indépendante, et le Haut Comité pour la transparence et l’information en matière de sécurité nucléaire. La loi prévoit l’établissement d’une convention entre l’IRSN et l’ASN pour définir les modalités de l’appui technique que l’institut fournit à celle-ci.
« Quels sont les enseignements d’INWORKS ? L’étude INWORKS est fondée sur la fusion de trois études préexistantes. Cette collaboration internationale a permis de vérifier et consolider les résultats suggérés antérieurement par chacune de ces trois études. L’étude INWORKS montre que, sur l’ensemble de la population d’INWORKS, la relation dose-réponse pour les cancers hors leucémies est statistiquement significative pour une exposition externe aux rayonnements ionisants étalée dans le temps (autrement dit chronique). Aux très faibles doses, c’est- à-dire en dessous de quelques dizaines de mSv, l’incertitude statistique devient importante, et la relation dose-réponse n’est plus statistiquement significative. L’association dose-risque observée dans l’étude INWORKS est cohérente avec celles observées dans d’autres études, en particulier chez les survivants des bombardements atomiques de Hiroshima et Nagasaki. Ces résultats sont compatibles avec l’une des hypothèses sous-jacentes au système de radioprotection actuel qui est l’extrapolation du modèle dérivé des survivants des bombardements de Hiroshima et Nagasaki aux populations exposées de façon répétée à de faibles doses. Ces résultats soutiennent la justification d’une protection radiologique des populations exposées aux faibles doses de rayonnements ionisants (travailleurs de l’industrie nucléaire, personnels médicaux, exposition médicale diagnostique…). »
L’étude INWORKS et son annexe sur Internet :
1 | www.thelancet.com/pdfs/journals/lanhae/PIIS2352-30264-0.pdf
2 | www.thelancet.com/cms/attachment/2033851355/2049708892/mmc1.pdf
1 Pour la France, selon l’OMS, 143 000 décès sont dus à des cancers sur un total de 499 000 décès annuels.
2 « Recommandations 2007 de la Commission internationale de protection radiologique » (publication 103), page 48.
3 Considérons deux solutions ERR1=aD et ERR2=bD l’écart entre les deux fonctions DERR=(a-b)D. L’écart quadratique, qui intervient dans la qualité des ajustements croît donc comme le carré de la dose D.
4 Le tableau précise aussi les domaines de validité de ces estimations (intervalle de confiance à 90 %). On constate que les marges d’erreur sont généralement considérables.
Publié dans le n° 316 de la revue
Partager cet article
L' auteur

Hervé Nifenecker
Hervé Nifenecker est physicien nucléaire et président d’honneur de Sauvons le Climat. Il est auteur de plusieurs (...)
Plus d'informationsNucléaire
Conséquences sanitaires de l’accident de Fukushima
Le 7 juin 2023
Les contaminations radioactives au tritium
Le 7 juin 2023
L’échelle INES des incidents et accidents nucléaires
Le 4 juin 2023













![[Conférence en ligne - 12 mars 2024 (20h)] Comment tripler la puissance nucléaire dans le monde en 2050 ?](local/cache-gd2/a0/cca2793d584ae4680a0810d51503a0.png?1709748010)